Olá, queridos estudantes e entusiastas da química! Hoje, vamos mergulhar em um fenômeno verdadeiramente cativante: a quimioluminescência. Preparem-se para descobrir como a luz pode ser produzida por uma reação química, enquanto exploramos o fascinante mundo das pulseiras fluorescentes.
A quimioluminescência é um processo químico no qual a energia liberada por uma reação resulta na emissão de luz visível. Ao contrário da bioluminescência, na qual organismos vivos produzem luz, a quimioluminescência ocorre em uma escala molecular. Essa propriedade intrínseca das substâncias quimioluminescentes torna-as um tema instigante para estudo e aplicação em diversas áreas da ciência.
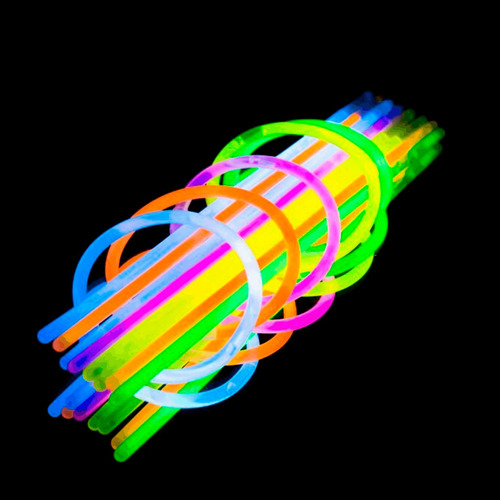
Uma das aplicações mais conhecidas da quimioluminescência está nas pulseiras fluorescentes que muitos de vocês já devem ter visto em festas ou eventos noturnos. Essas pulseiras contêm uma substância chamada luminol, que é responsável por seu brilho característico. Vamos descobrir como a reação química do luminol pode nos fornecer uma fonte de luz impressionante!
A reação química na pulseira fluorescente envolve a mistura do luminol (C8H7O2N3) com um oxidante, geralmente o peróxido de hidrogênio, que está presente em uma cápsula interna. Quando essa cápsula é quebrada, o peróxido de hidrogênio entra em contato com o luminol e inicia a reação. A energia liberada durante essa reação é convertida em luz, resultando em uma brilhante luminescência.
A reação química do luminol com o peróxido de hidrogênio ocorre em várias etapas. Primeiro, o peróxido de hidrogênio fornece oxigênio ativado (O2*) através da sua decomposição catalisada pelo luminol. O oxigênio ativado, por sua vez, reage com o luminol, resultando na formação de um estado excitado do luminol. Esse estado excitado é instável e rapidamente volta ao seu estado fundamental, liberando energia na forma de luz visível.
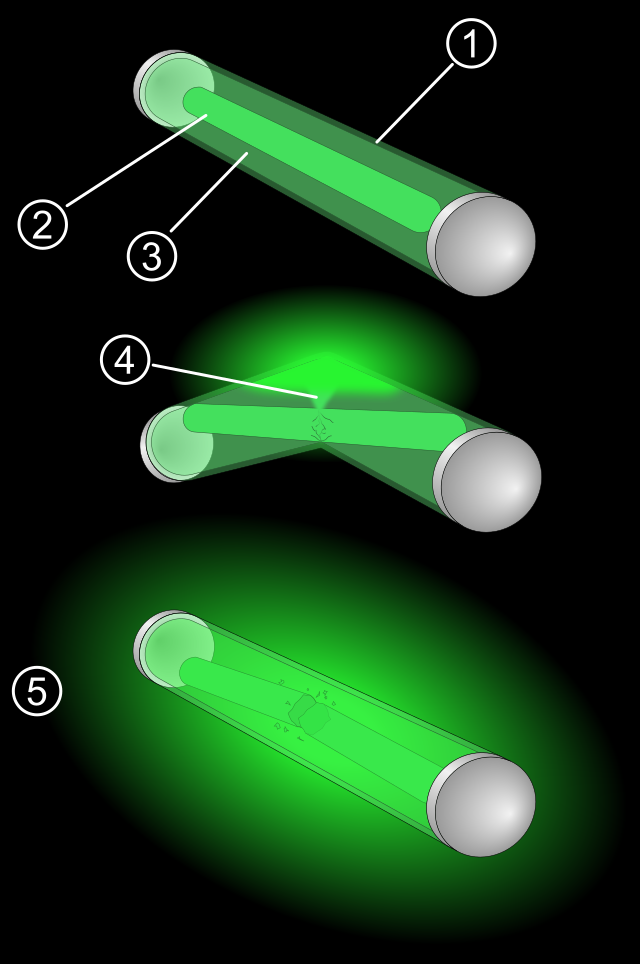
- Uma cápsula de plástico envolve o luminol e a ampola de vidro.
2. Uma ampola de vidro envolve a água oxigenada.
3. Solução de luminol e algum corante.
4. A dobra da pulseira quebra a ampola de vidro a as duas soluções reagem.
5. Durante a reação a pulseira começa a brilhar.Fonte: Wikipedia
É importante ressaltar que a cor da luz emitida pode variar dependendo dos componentes adicionais presentes na pulseira fluorescente. Por exemplo, a adição de corantes fluorescentes pode conferir diferentes tonalidades à luz emitida. Essa propriedade é explorada em outros dispositivos quimioluminescentes, como lanternas de emergência e marcadores de sinalização.
Além das pulseiras fluorescentes, a quimioluminescência tem aplicações em diversas áreas da ciência, como na análise de DNA, no estudo de processos bioquímicos e na pesquisa de medicamentos. A capacidade de detectar e medir a luz emitida durante uma reação quimioluminescente é utilizada em laboratórios para análises e diagnósticos sensíveis.
Portanto, a quimioluminescência é um fenômeno cativante que nos permite explorar a conexão entre a química e a luz.
![]()
Fonte da imagem: https://www.scielo.br/j/ciedu/a/gJsCwzN8yCbWvhrJpKSHMKg/
Continuando nosso mergulho na quimioluminescência, vamos explorar a fórmula da reação química que ocorre na pulseira fluorescente com luminol. É importante lembrar que a reação é simplificada para fins didáticos, e na prática existem outras substâncias e processos envolvidos.
Aqui está a fórmula geral da reação química da quimioluminescência com luminol e peróxido de hidrogênio:
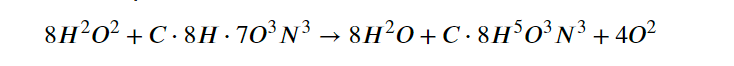
Nessa equação, o peróxido de hidrogênio (H2O2) atua como oxidante e fornece o oxigênio ativado (O2*), que é fundamental para a emissão de luz. O luminol (C8H7O3N3) é a substância quimioluminescente, que passa por um processo de excitação e retorna ao seu estado fundamental, liberando energia na forma de luz. A água (H2O) é um dos produtos da reação.
No entanto, é importante ressaltar que a reação quimioluminescente do luminol é influenciada por diversos fatores, como a concentração dos reagentes, a temperatura e o pH do meio. Esses parâmetros podem ser ajustados para otimizar a intensidade e a duração da luminescência.
Embora a fórmula química nos dê uma ideia da natureza dos reagentes e produtos envolvidos na reação, a quimioluminescência é um processo complexo que envolve transferência de energia e interações moleculares específicas. A compreensão completa desses mecanismos requer conhecimentos avançados de química física e fotoquímica.
A quimioluminescência é um exemplo fascinante de como a química pode nos proporcionar fenômenos luminosos surpreendentes. Através das pulseiras fluorescentes e de outros dispositivos quimioluminescentes, podemos apreciar a beleza da luz gerada pela ciência. Esses estudos e aplicações da quimioluminescência nos permitem compreender melhor as reações químicas e explorar suas implicações em diversas áreas, desde a pesquisa científica até a indústria e a medicina.
Espero que esse mergulho na quimioluminescência tenha sido tão empolgante para vocês quanto foi para mim! A química é realmente fascinante e está repleta de maravilhas para serem descobertas. Fiquem curiosos e continuem explorando os segredos da ciência!









